- Γράφει ο Κοσμάς Ζακυνθινός
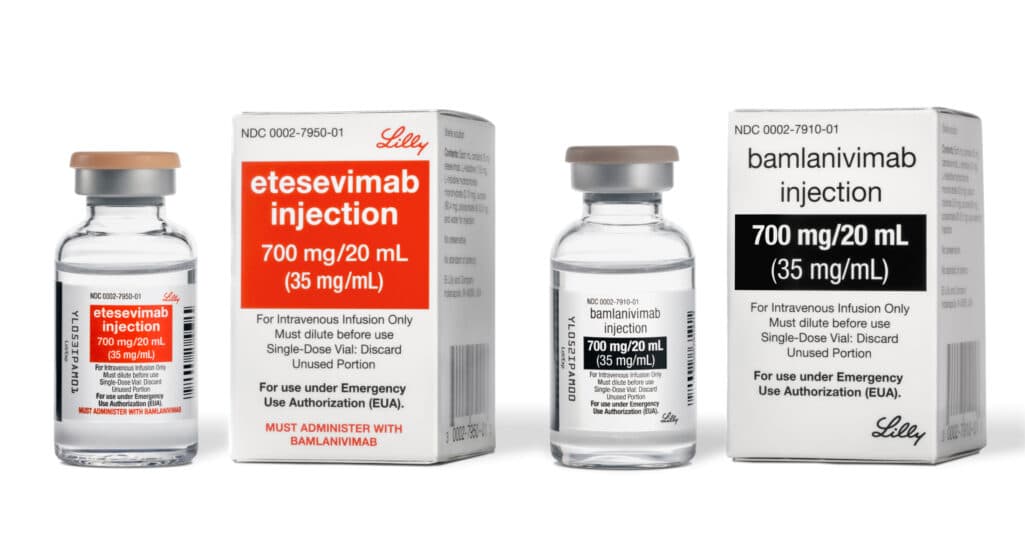
«Πράσινο φως» έδωσε ο Αμερικανικός Οργανισμός Τροφίμων και Φαρμάκων (Food and Drug Administration – FDA) για την κατεπείγουσα χρήση συνδυαστικής θεραπείας δύο συνθετικών αντισωμάτων (bamlanivimab – etesevimab) την οποία έχει αναπτύξει η φαρμακευτική Eli Lilly για την αντιμετώπιση της COVID-19, της νόσου που προκαλεί ο νέος κορωνοϊός.
Η συνδυαστική θεραπεία δύο συνθετικών αντισωμάτων, της μπαμλανιβιμάμπης (bamlanivimab) και της ετεσεβιμάμπης (etesevimab), συνέβαλε να μειωθούν κατά 70% οι νοσηλείες και οι θάνατοι μεταξύ ασθενών που ανήκουν σε κατηγορίες υψηλού κινδύνου, κατά δεδομένα μιας κλινικής μελέτης που παρουσίασε η εταιρεία στα τέλη του Ιανουαρίου.
Η θεραπεία «εγκρίθηκε για τη θεραπεία ήπιας ως μέτριας (μορφής του) COVID-19 σε ασθενείς ηλικίας 12 (ετών) και άνω που υπάρχει υψηλός κίνδυνος να παρουσιάσουν πολύ σοβαρή (μορφή του) COVID-19 ή/και (να χρειαστούν) νοσηλεία», όπως τονίζει η Eli Lilly.
Μειωμένος χρόνος έγχυσης
Επιπλέον, o FDA ενέκρινε τους μειωμένους χρόνους έγχυσης για το bamlanivimab και το συνδυασμό bamlanivimab και etesevimab στα 16 ή 21 λεπτά αντίστοιχα. Πρόκειται για μια σημαντική μείωση από τον προηγούμενο εγκεκριμένο χρόνο των 60 λεπτών. Η απόφαση έρχεται ως «απάντηση» στα σχόλια που ελήφθησαν από νοσοκόμες και γιατρούς πρώτης γραμμής που. χορηγούν αυτές τις εγχύσεις και αποσκοπούν στη μείωση των πιέσεων που δέχεται το σύστημα υγειονομικής περίθαλψης.
«Στην Eli Lilly έχουμε αφιερώσει χρόνο, πόρους και αξιοποιήσαμε συστήματα τεχνογνωσίας για να ανακαλύψουμε και να αναπτύξουμε θεραπείες κατά της νόσου COVID-19», όπως σημείωσε ο κ. Ντάνιελ Σκοβρόνσκι, MD, Ph.D., Διευθύνων Σύμβουλος και Πρόεδρος των Ερευνητικών Εργαστηρίων της Eli Lilly.
«Το bamlanivimab, που χορηγείται με άδεια έκτακτης ανάγκης έχει ήδη αποτελέσει για πολλούς ασθενείς επιλογή πρώιμης θεραπείας, που θα μπορούσε να αποτρέψει τις νοσηλείες. Είμαστε ενθουσιασμένοι που τώρα προσθέτουμε μια επιπλέον θεραπευτική επιλογή με παρόμοιο αποδεδειγμένο κλινικό όφελος. Επιπλέον, δεδομένου του κινδύνου εμφάνισης αντίστασης στα διάφορα στελέχη που προκύπτουν από τον ιό, το. bamlanivimab και το etesevimab μαζί θα μπορούσαν ενδεχομένως να είναι. αποτελεσματικά σε ένα ευρύτερο φάσμα παραλλαγών του SARS-CoV-2», υπογράμμισε ο κ. Ντάνιελ Σκοβρόνσκι.
Ένα εκατομμύριο δόσεις
Το bamlanivimab μόνο του έχει εγκριθεί σε πολλές χώρες. Ενώ, το bamlanivimab και το etesevimab είναι προς το παρόν εγκεκριμένα στις ΗΠΑ και την Ιταλία. Η Lilly θα συνεχίσει να συνεργάζεται με παγκόσμιους ρυθμιστές για να καταστήσει αυτές τις θεραπείες διαθέσιμες σε όλο τον κόσμο.
Σε μια προσπάθεια να βοηθήσει όσο το δυνατόν περισσότερους ασθενείς, η Lilly θα συνεχίσει να προμηθεύει το bamlanivimab σύμφωνα με τις άδειες που χορηγούνται σε διάφορες χώρες, ενώ συνεχίζει να επιταχύνει την παρασκευή του etesevimab για χρήση σε όλο τον κόσμο. Η Lilly, σε συνεργασία με την Amgen, σχεδιάζει να παράγει έως 1 εκατομμύριο δόσεις etesevimab για χορήγηση με bamlanivimab έως τα μέσα του 2021.
Κάντε like στη σελίδα μας στο facebook για να μαθαίνετε όλα τα νέα